- 广东省医疗器械网络交易服务第三方平台备案办理
- 海南省医疗器械网络交易服务第三方平台备案办理
- 北京市医疗器械网络交易服务第三方平台备案办理
- 天津市医疗器械网络交易服务第三方平台备案办理
- 河北省医疗器械网络交易服务第三方平台备案办理
- 山西省医疗器械网络交易服务第三方平台备案办理
- 内蒙古医疗器械网络交易服务第三方平台备案办理
- 辽宁省医疗器械网络交易服务第三方平台备案办理
- 吉林省医疗器械网络交易服务第三方平台备案办理
- 黑龙江省医疗器械网络交易服务第三方平台备案办理
- 上海市医疗器械网络交易服务第三方平台备案办理
- 江苏省医疗器械网络交易服务第三方平台备案办理
- 浙江省医疗器械网络交易服务第三方平台备案办理
- 安徽省医疗器械网络交易服务第三方平台备案办理
- 福建省医疗器械网络交易服务第三方平台备案办理
- 江西省医疗器械网络交易服务第三方平台备案办理
- 山东省医疗器械网络交易服务第三方平台备案办理
- 河南省医疗器械网络交易服务第三方平台备案办理
- 陕西省医疗器械网络交易服务第三方平台备案办理
- 甘肃省医疗器械网络交易服务第三方平台备案办理
- 青海省医疗器械网络交易服务第三方平台备案办理
- 宁夏医疗器械网络交易服务第三方平台备案办理
- 新疆医疗器械网络交易服务第三方平台备案办理
- 湖北省医疗器械网络交易服务第三方平台备案办理
- 湖南省医疗器械网络交易服务第三方平台备案办理
- 重庆市医疗器械网络交易服务第三方平台备案办理
- 贵州省医疗器械网络交易服务第三方平台备案办理
- 四川省医疗器械网络交易服务第三方平台备案办理
- 云南省医疗器械网络交易服务第三方平台备案办理
- 西藏医疗器械网络交易服务第三方平台备案办理
- 广西医疗器械网络交易服务第三方平台备案办理
- 中国医疗器械
- 美国医疗器械
- 加拿大医疗器械
- 欧洲医疗器械
- 英国医疗器械
- 巴西医疗器械
- 澳大利医疗器械
- 俄罗斯医疗器械
- 日本医疗器械
- 韩国医疗器械
- 印度医疗器械
- 德国医疗器械
- 厄尔多瓜医疗器械注册
- 印尼医疗器械
- 墨西哥医疗器械
- 巴基斯坦医疗器械
- 埃俄比亚医疗器械
- 新加坡医疗器械
- 哥伦比亚医疗器械
- 印度尼西亚医疗器械
- 中国香港医疗器械
- 马来西亚医疗器械
- 新西兰医疗器械
- 阿联酋医疗器械
- 越南医疗器械
- 南非医疗器械
- 泰国医疗器械
- 土耳其医疗器械
关于快可利
深圳快可利信息技术有限公司发起成立的生物医药产业服务联盟,整合了国内外从事生物医药产业化服务的十几家专业单位和各种资源,形成了从工程设计、施工改造、全球产品注册和临床指导、GMP认证辅导、专业培训、验厂咨询、符合性工厂审计到医药技术服务平台的生物医药全程服务体系和整体解决方案。管理咨询核心业务是良好生产质量管理规范(GMP)认证辅导,执行标准包括:中国/美国/欧盟及全球药品GMP和原料药Q7,医疗器械ISO13485/QSR820/中国医疗器械GMP,中国保健食品GMP及美国食品/营养补充剂GMP、全球食品ISO22000、BRC、IFS等,欧盟/美国/东盟化妆品GMP及全球化妆品GMP(即ISO22716)等。

关于快可利
深圳快可利信息技术有限公司发起成立的生物医药产业服务联盟,整合了国内外从事生物医药产业化服务的十几家专业单位和各种资源,形成了从工程设计、施工改造、全球产品注册和临床指导、GMP认证辅导、专业培训、验厂咨询、符合性工厂审计到医药技术服务平台的生物医药全程服务体系和整体解决方案。管理咨询核心业务是良好生产质量管理规范(GMP)认证辅导,执行标准包括:中国/美国/欧盟及全球药品GMP和原料药Q7,医疗器械ISO13485/QSR820/中国医疗器械GMP,中国保健食品GMP及美国食品/营养补充剂GMP、全球食品ISO22000、BRC、IFS等,欧盟/美国/东盟化妆品GMP及全球化妆品GMP(即ISO22716)等。

关于快可利
深圳快可利信息技术有限公司发起成立的生物医药产业服务联盟,整合了国内外从事生物医药产业化服务的十几家专业单位和各种资源,形成了从工程设计、施工改造、全球产品注册和临床指导、GMP认证辅导、专业培训、验厂咨询、符合性工厂审计到医药技术服务平台的生物医药全程服务体系和整体解决方案。管理咨询核心业务是良好生产质量管理规范(GMP)认证辅导,执行标准包括:中国/美国/欧盟及全球药品GMP和原料药Q7,医疗器械ISO13485/QSR820/中国医疗器械GMP,中国保健食品GMP及美国食品/营养补充剂GMP、全球食品ISO22000、BRC、IFS等,欧盟/美国/东盟化妆品GMP及全球化妆品GMP(即ISO22716)等。

快可利新闻 快可利公告
- 江苏xxx制造有限公司ISO9001:2015质量体系认证项目于2021年5月17日正式启动 2023-11-06
- 扬州xxx机械制造有限公司ISO9001:2015质量体系认证项目于2020年6月18日正式启动 2023-11-06
- 台山市xxx制造有限公司ISO9001:2015质量体系认证项目于2021年5月27日正式启动 2023-11-06
- 宁波市xxx真空设备厂ISO9001:2015质量体系认证项目于2022年2月25日正式启动 2023-11-06
- 苏州XXX工程有限公司ISO9001:2015质量体系认证项目于2021年7月28日正式启动 2023-11-06
- 苏州XXX电子有限公司ISO9001:2015质量体系认证项目于2021年7月29日正式启动 2023-11-03
- 无锡市xxx配件厂ISO9001:2015质量体系认证项目于2020年8月3日正式启动 2023-11-03
- 宁波XXX设备有限公司ISO9001:2015质量体系认证项目于2020年8月25日正式启动 2023-11-03
- 张家港市XXX纺织有限公司ISO9001质量体系认证项目于2020年4月22日正式启动 2023-11-03
- 东莞市xxx皮具有限公司ISO9001质量体系项目于2019年11月20日正式启动 2023-11-03
- 2023 年“中秋&国庆”节放假通知 2023-10-30
行业动态 学术论坛
- 医疗器械标准高质量发展交流会在京召开 2024-10-15
- 关于《采用脑机接口技术的医疗器械 术语及定义》等2项医疗器械行业标准立项的通知 2024-10-09
- 创新医疗器械产品注册代办|创新药品和医疗器械上市步伐加快 促进医药产业高质量发展 2024-09-23
- 医疗器械产品注册证代办服务|我国将进一步加快临床急需创新药和医疗器械的审评审批 2024-09-23
- 医疗器械管理法咨询|中华人民共和国医疗器械管理法 (草案征求意见稿) 2024-09-14
- 医疗器械注册管理咨询|我国首部医疗器械管理法雏形初现 2024-09-14
- 医疗器械生产许可证代办|云南省关于做好应急审批医疗器械延续注册与生产许可衔接工作的通知 2024-09-13
- GMP认证辅导|云南省药品监督管理局促进医疗器械产业高质量发展20条措施 2024-09-13
- 医疗器械产品注册证代理机构|《黑龙江省药品监督管理局关于进一步做好医疗器械注册备案管理工作的通知》的政策解读 2024-08-19
- 医疗器械生产许可证代办服务|黑龙江省药监局推进“两品一械”电子证照应用推广工作方案 2024-08-19
- FDA注册咨询|美国发布人工智能与医疗产品协同工作报告 2024-11-05
- IVD注册证代办服务|校准品注册上市情况与审评关注要点 2024-11-05
- 医疗器械产品注册咨询|一次性使用血液灌流器注册监管思考 2024-09-23
- 医疗器械产品注册证代办服务|口腔修复用增材制造金属材料性能评价及思考 2024-08-12
- 医疗器械产品注册证代办|口腔修复用增材制造金属材料性能评价及思考 2024-08-09
- 医疗器械产品注册证代理服务|分子诊断学技术全方面概述说明 2024-07-19
- 医疗器械产品注册申请机构|遇到技术和法规问题,有哪些途径可以寻求答案? 2024-07-01
- 医疗器械/体外诊断试剂产品临床试验咨询|开展临床试验可参考技术文件汇总 2024-07-01
- 医疗器械产品分类界定|新产品如何确定分类|产品注册申请要求 2024-07-01
- 医疗器械产品注册证代办机构|注册申报一个医疗器械产品所需的时长 2024-07-01
- 解决方案
.e60271e.png) 产品注册 产品注册注意事项想为。。。。。。undefinedundefined1,这是1点undefinedundefined2,这是两点undefinedundefined3,这是三点undefined
产品注册 产品注册注意事项想为。。。。。。undefinedundefined1,这是1点undefinedundefined2,这是两点undefinedundefined3,这是三点undefined.c944dfd.png) 产品认证 洁净室最主要之作用在于控制产品所接触之大气的洁净度日及温湿度,使产品能在一个良好之环境空间中生产、制造,此空间我们称之为洁净室。
产品认证 洁净室最主要之作用在于控制产品所接触之大气的洁净度日及温湿度,使产品能在一个良好之环境空间中生产、制造,此空间我们称之为洁净室。.5c9c52e.png) 产品检测 洁净室最主要之作用在于控制产品所接触之大气的洁净度日及温湿度,使产品能在一个良好之环境空间中生产、制造,此空间我们称之为洁净室。
产品检测 洁净室最主要之作用在于控制产品所接触之大气的洁净度日及温湿度,使产品能在一个良好之环境空间中生产、制造,此空间我们称之为洁净室。.ad5989a.png) 生产企业生产备案/许可 洁净室最主要之作用在于控制产品所接触之大气的洁净度日及温湿度,使产品能在一个良好之环境空间中生产、制造,此空间我们称之为洁净室。
生产企业生产备案/许可 洁净室最主要之作用在于控制产品所接触之大气的洁净度日及温湿度,使产品能在一个良好之环境空间中生产、制造,此空间我们称之为洁净室。
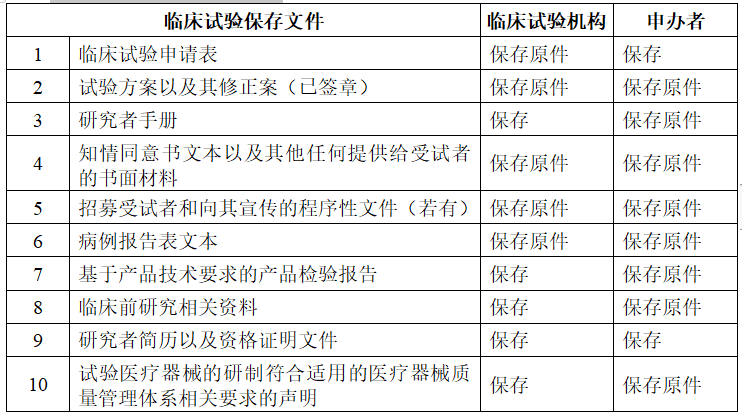
医疗器械/体外诊断试剂临床试验基本文件目录-临床试验完成或者终止后
发布时间:2023-08-15 文章来源:国家药监局 阅读人数:138 微信 贴吧 QQ空间 邮箱






为指导申办者和医疗器械临床试验机构开展医疗器械(含体外诊断试剂,下同)临床试验,特制定本文件目录供参考执行。
医疗器械临床试验开展顺序一般为:申办者完成临床前相关研究,选择已备案的医疗器械临床试验机构以及主要研究者,并组织临床试验方案等相关文件制定。伦理委员会审查批准该临床试验,申办者与临床试验机构签订合同后进行医疗器械临床试验项目备案;其中,对人体具有较高风险的第三类医疗器械临床试验,还应当经国务院药品监督管理部门批准。受试者签署知情同意书以及入组,研究者按照临床试验方案实施临床试验。申办者在临床试验完成后向所在地省局报告。
三、临床试验完成或者终止后
- 热门文章12

医疗器械注册证代办-关于修改并继续执行《山东省医疗器械不良事件风险预警管理办法》政策解读
- 医疗器械注册证代办服务-山东省医疗器械不良事件风险预警管理办法
- 吉林省药品监督管理局2024年度法治政府建设工作报告
- 医疗器械注册管理工作片区座谈会召开
- 2024医疗器械经济信息发布会在上海召开
- FDA注册咨询|美国发布人工智能与医疗产品协同工作报告
- IVD注册证代办服务|校准品注册上市情况与审评关注要点
- 医疗器械产品注册证代办|医疗器械警戒试点工作推进会召开
- 医疗器械标准高质量发展交流会在京召开
- 关于《采用脑机接口技术的医疗器械 术语及定义》等2项医疗器械行业标准立项的通知
- 创新医疗器械产品注册代办|创新药品和医疗器械上市步伐加快 促进医药产业高质量发展
- 热门项目
.36720e2.png)
在线咨询

陈老师


徐老师


王小姐


郭小姐

.2f44860.png)
热线电话
 18576401396
18576401396  18575592846
18575592846 .43b2c75.png)
转发网站



微信

贴吧

QQ空间

邮箱

.4f4ea8a.png)
在线留言
.a3a1a2a.png)
回到顶部
 请您留言
请您留言

.3263ff2.png)
.0d83381.png)
.dec0422.png)






